Detrás de la dureza de una espada samurái o de la robustez de una viga que sostiene un rascacielos, se esconde una ciencia tan compleja como fascinante. Pocas personas se detienen a pensar que el acero, ese material omnipresente, es el resultado de una alquimia moderna donde la física, la química y la ingeniería dialogan en un lenguaje que mezcla átomos, calor y tiempo.
No hablamos simplemente de hierro reforzado. El acero es una sinfonía de estructuras microscópicas, de fases que aparecen y desaparecen según cómo se enfríe o se caliente el material, de decisiones que parecen invisibles pero que determinan su destino. Cada herramienta que resiste la fricción, cada pieza de un motor que desafía la presión o cada hoja que mantiene su filo en la batalla, es el resultado de una historia que empieza mucho antes de su uso final. Es en esa historia donde vamos a sumergirnos.
Todo comienza con una danza. En estado líquido, los átomos de hierro y carbono se mueven libremente, como en una coreografía sin dirección. Pero cuando el metal comienza a enfriarse, esa libertad se transforma en orden. Los átomos buscan acomodarse en patrones estables y nacen los primeros cristales. Este proceso no ocurre desde un solo punto, sino desde muchos, simultáneamente. Así surgen los granos: pequeñas regiones donde los átomos se alinean de una forma particular, cada una con su orientación.
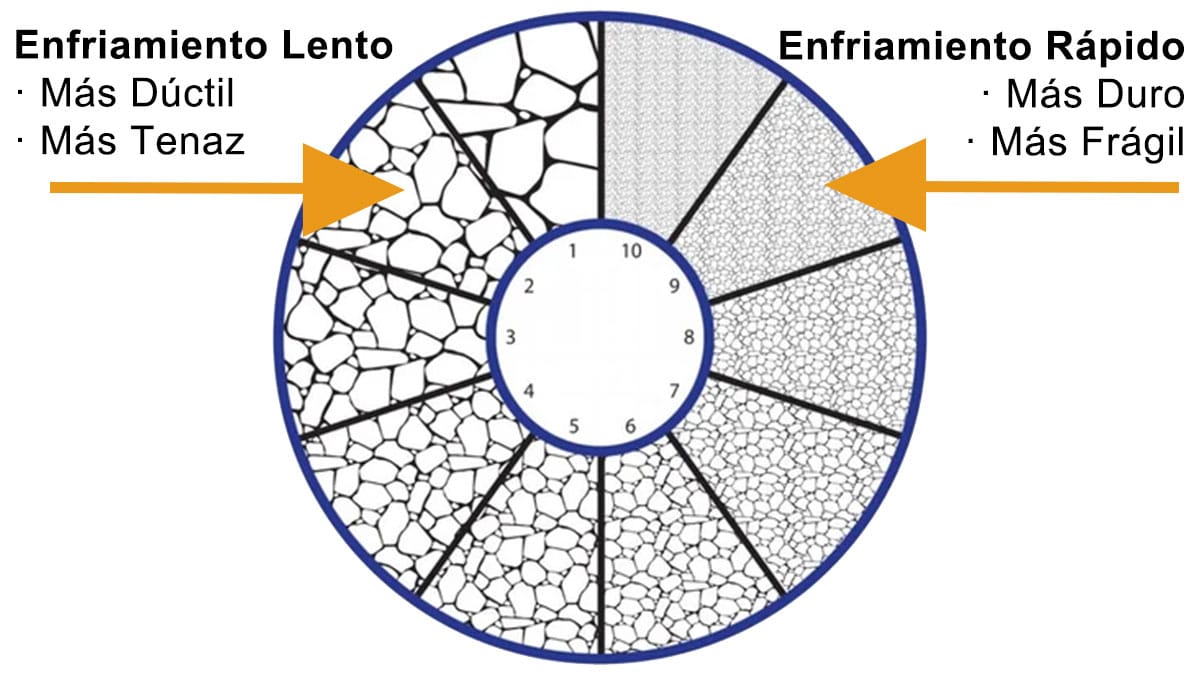
Cuando dos de estos granos se encuentran, los átomos ya no encajan con la misma armonía. Aparecen los límites de grano, zonas de transición donde la estructura se vuelve más caótica, más vulnerable. Y aquí empieza el juego del control. Si el enfriamiento es lento, los granos tienen tiempo de crecer, de extenderse con calma. El resultado es un acero más dúctil, más tenaz, capaz de absorber impactos sin quebrarse. En cambio, si el metal se enfría con rapidez, los granos apenas tienen tiempo de formarse antes de verse congelados en su lugar. El material se vuelve más duro, más resistente al desgaste, pero también más frágil ante golpes inesperados. Este delicado equilibrio entre dureza y ductilidad define muchas de las decisiones en la fabricación del acero.
Para dominar esta complejidad, los ingenieros recurren a un instrumento indispensable: el diagrama de fases. Es, en esencia, un mapa que describe qué ocurre con el acero según su temperatura y su composición química. En sistemas simples, como el cobre con níquel, este mapa es casi lineal. Los átomos se sustituyen sin mayores conflictos, y las fases transitan suavemente de una a otra.
Pero el acero no es un sistema simple. El carbono no reemplaza al hierro; se cuela entre sus átomos, forzando su entrada en huecos que apenas lo toleran. Esta intrusión genera tensiones internas, rompe simetrías y hace que las transiciones entre fases sean complejas, impredecibles y profundamente influyentes en las propiedades finales del material. Por eso, el diagrama hierro-carbono es mucho más que una herramienta técnica: es una brújula para transformar la materia.
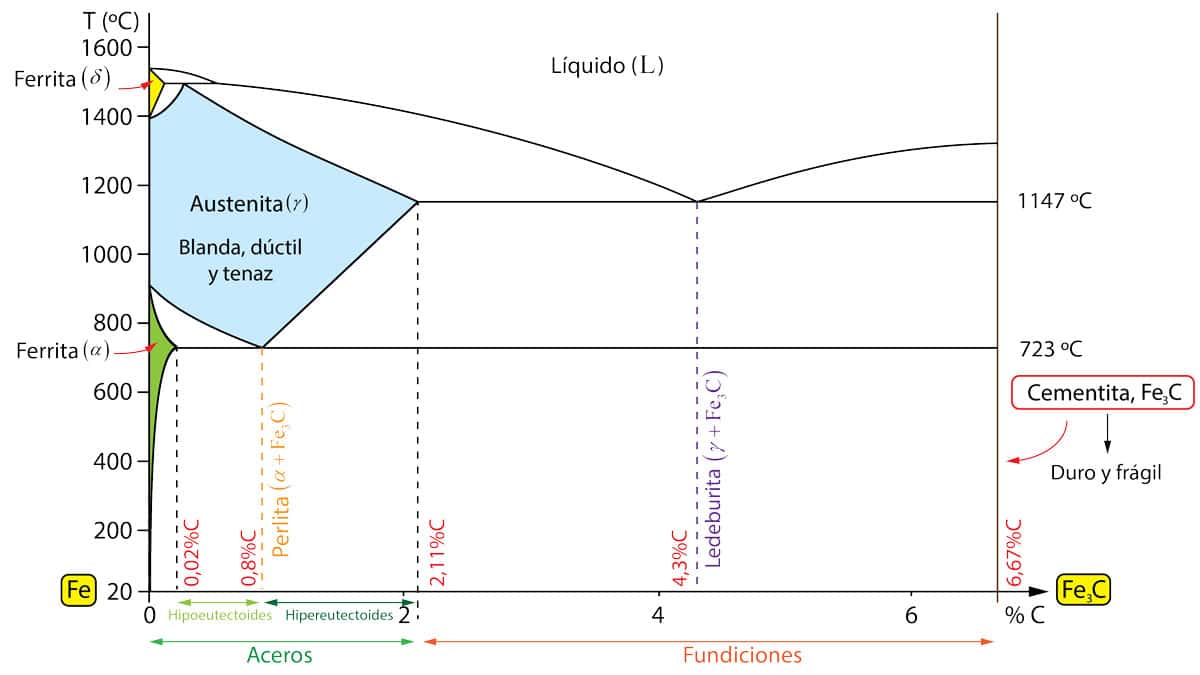
En ese universo de fases hay nombres que parecen salidos de un libro de magia: ferrita, austenita, cementita, perlita, martensita, bainita. Cada una tiene su estructura, su temperatura de aparición, su papel en la historia térmica del acero. La ferrita es la forma más estable del hierro a temperatura ambiente: blanda, magnética, con una estructura cúbica centrada en el cuerpo. Apenas puede disolver carbono, pero su ductilidad la hace indispensable.
Cuando el acero se calienta por encima de los 727 °C, entra en escena la austenita. Su estructura cambia: se vuelve más abierta, cúbica centrada en las caras, y de pronto el carbono encuentra más espacio donde alojarse. Esta fase es clave, porque es la puerta de entrada a muchas transformaciones. Al enfriarse desde esta etapa, el acero puede derivar en perlita si el proceso es lento, o en martensita si es abrupto. Entre ambos extremos puede surgir la bainita, que combina dureza y tenacidad como pocas estructuras pueden hacerlo.
La cementita, en cambio, no es una fase intermedia. Es un compuesto químico: carburo de hierro. Su dureza es altísima, pero también su fragilidad. Cuando se forma, marca un límite en la ductilidad del material. Su presencia, en equilibrio con la ferrita o en mezcla con la austenita, es responsable de muchas de las propiedades mecánicas del acero.
Imaginemos un acero con un contenido de carbono del 0,77 %, lo que se conoce como un acero eutectoide. Si se calienta a 1.600 °C, se encuentra en estado líquido. A medida que la temperatura baja, se solidifica en forma de austenita. Y cuando alcanza los 727 °C, esa austenita se descompone, no en una sola fase, sino en una mezcla perfectamente ordenada: la perlita, compuesta por láminas alternas de ferrita y cementita. Este momento, invisible al ojo humano, define las características esenciales del acero.
No es solo una cuestión de temperaturas. La velocidad con la que se enfría también importa. Un enfriamiento rápido puede impedir que los átomos encuentren su posición en las fases de equilibrio. En lugar de perlita, se forma martensita: una estructura endurecida, casi cristalina, donde el carbono queda atrapado en una posición forzada. Es extremadamente dura, ideal para filos de cuchillos o herramientas de corte, pero también propensa a fracturarse si se somete a impactos.
Aquí es donde la metalurgia se convierte en arte. Mediante los tratamientos térmicos, el acero puede ser transformado casi a voluntad. El templado, por ejemplo, es una técnica que consiste en calentar el acero hasta la fase austenítica y luego enfriarlo de forma rápida. Esto provoca la formación de martensita. Pero la martensita, por su dureza extrema, también encierra tensiones internas. Si no se maneja bien, puede provocar grietas o fracturas. Por eso, a menudo se realiza un revenido posterior: se vuelve a calentar, pero a temperaturas más bajas, para aliviar esas tensiones y equilibrar dureza con tenacidad.
Otra técnica es el normalizado, que busca homogeneizar la estructura. El acero se calienta y se deja enfriar al aire, lo que permite obtener una microestructura más equilibrada, generalmente perlítica o bainítica. Este proceso es esencial cuando se busca resistencia sin comprometer la capacidad de absorción de energía.
El recocido, por su parte, es el tratamiento más relajado. Se calienta el acero y se deja enfriar muy lentamente, permitiendo que los granos crezcan y se acomoden con tranquilidad. El resultado es un material más blando, más fácil de trabajar, ideal para etapas posteriores como el mecanizado o el conformado.
Pero el acero no es solo hierro y carbono. Su verdadero poder se revela cuando se le añaden otros elementos, en proporciones precisas, para modificar sus propiedades. Si se incorpora cromo, el acero se vuelve resistente a la oxidación. Es el nacimiento del acero inoxidable. Si se añade molibdeno o tungsteno, gana resistencia al calor y al desgaste, cualidades indispensables en herramientas de corte o componentes expuestos a fricción constante.
Cada elemento tiene un papel distinto. El vanadio afina el tamaño de grano, aumentando la resistencia. El níquel mejora la tenacidad en ambientes fríos. El manganeso refuerza la dureza sin comprometer la ductilidad. En conjunto, estas aleaciones permiten diseñar aceros a medida, verdaderos materiales de ingeniería que responden a exigencias específicas en campos tan variados como la automoción, la construcción, la energía o la medicina.
Quizá lo más asombroso del acero no sea su resistencia, ni su capacidad de transformación, sino su versatilidad. Es un material que puede ser tan blando como para doblarse con las manos o tan duro como para perforar otros metales. Puede resistir el tiempo, el calor, la corrosión, los impactos. Puede tomar formas delicadas o estructuras colosales. Desde una aguja quirúrgica hasta una torre de cientos de metros, el acero está presente como el esqueleto invisible del mundo moderno.
Y todo esto se logra con la combinación precisa de temperatura, composición química, velocidad de enfriamiento y, sobre todo, conocimiento. Entender la compleja ciencia del acero no solo permite manipularlo con precisión. También es una puerta de entrada a uno de los materiales más importantes de la historia humana. Un material cuya historia, aunque a veces invisible, sostiene buena parte de nuestras vidas.